Medidata eTMF
治験マスターファイル(TMF)を査察に対応できる状態に保つには、単に文書を保管するだけでは不十分です。チームは、絶え間ない手作業によるチェックや照合を行うことなく、TMFの内容が治験で実際に起きていることを反映しているという確信を持つ必要があります。
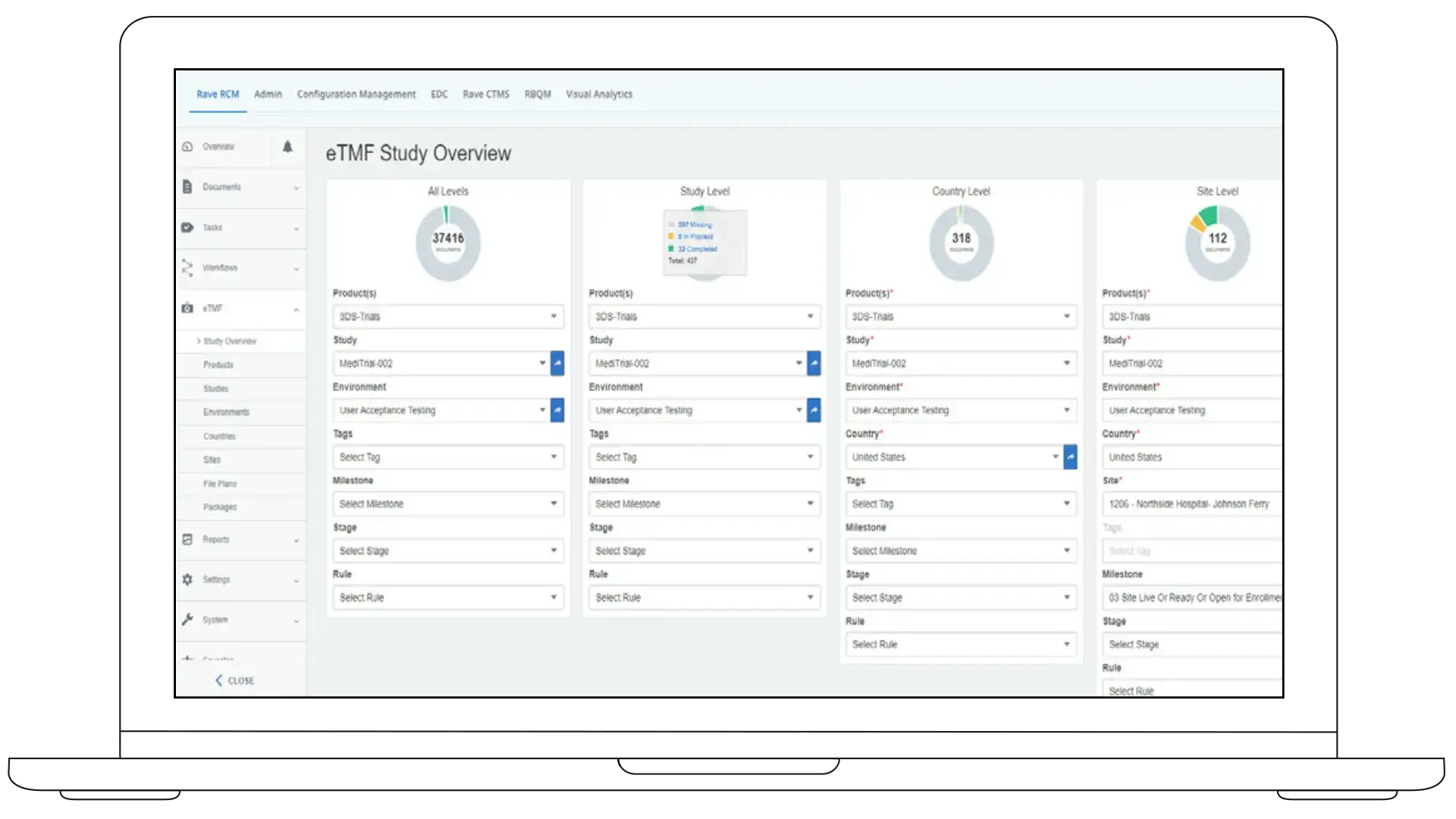
Medidata eTMFは、治験業務の完了に合わせて自動的に更新されるため、治験の規模拡大に伴うレビューやファイリング管理の手間を削減します。

大規模なオーバーサイト業務を簡素化
Medidata eTMFは、査察への対応を継続的なタスクではなく、デフォルトの状態にします。手作業のステップを削減し、治験ライフサイクル全体で文書のステータスを明確に保つことで、チームはTMFの管理に費やす時間を減らし、治験のオーバーサイトにより多くの時間を費やすことができます。
TMSステータスの明確な可視化
治験の進行に合わせたTMFの自動更新
ライブTMF移行サポート
リアルタイムのオーバーサイト
シンプルな治験から複雑な治験までサポート
Medidata eTMFで得られるメリット
複雑性の軽減
自動化されたワークフローで時間を短縮
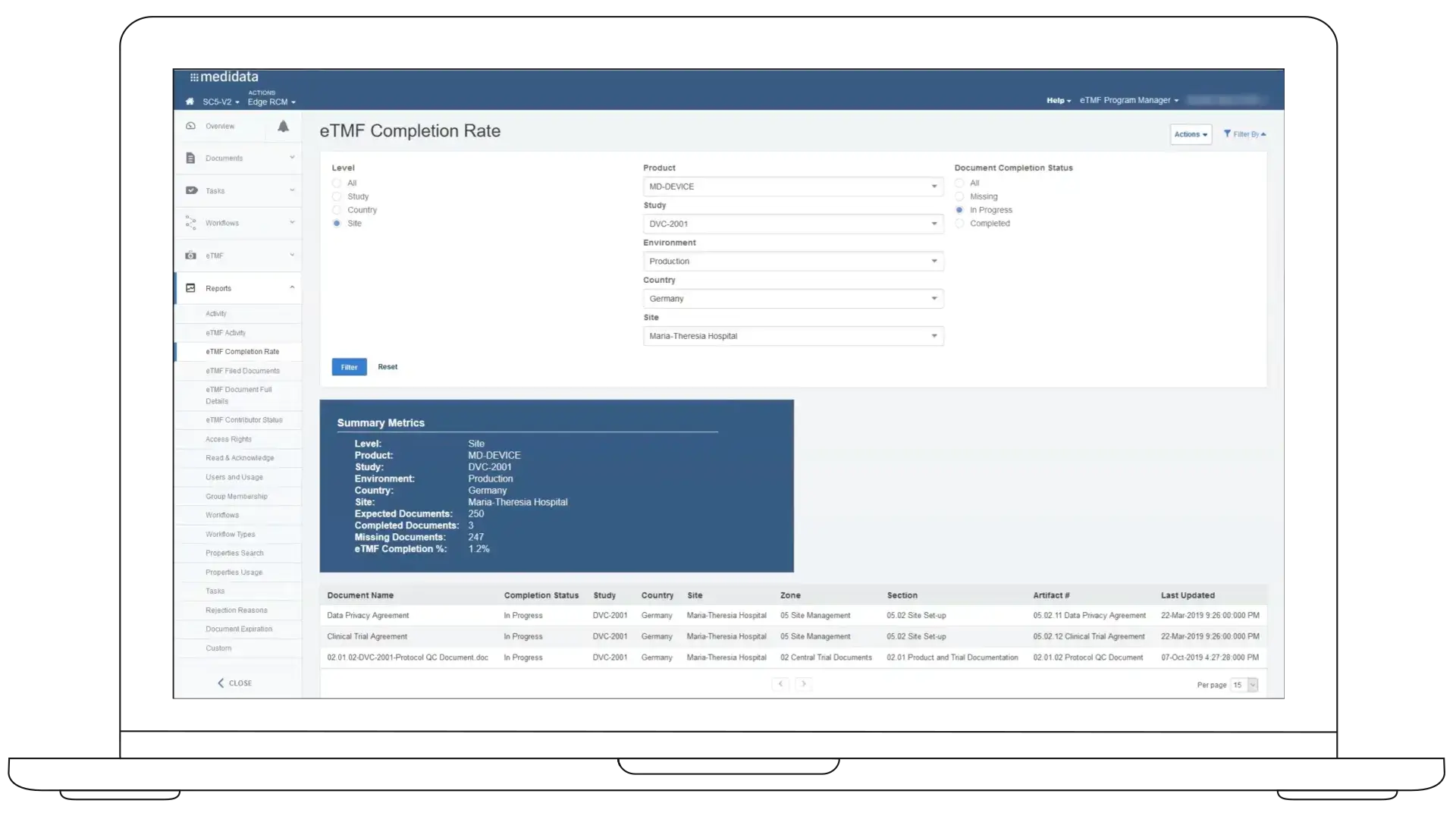
Rave EDCとMedidata CTMSでの作業が完了すると、文書とメタデータが自動的に入力され、手作業によるファイリングや照合を最小限に抑えられます。
自動ファイリング、標準化された構造、インテリジェントなプレースホルダーにより、追加の調整作業なしに必要な文書が作成・整理されるため、チームは管理業務ではなくオーバーサイト業務に集中できます。
注目のリソース
小規模チーム向けの自動化されたTMFワークフロー
確認書、報告書、監督状況の更新などの管理は、小規模チームにとってすぐに大きな負担となり得ます。Enterin社がMedidata eTMFを活用し、TMFワークフローの自動化、モニタリングの効率化、手作業の削減を実現した事例をご覧ください。実施医療機関の負担を軽減しながら、週に5~6時間を節約しています。
ケーススタディを読む
FAQ
Experienceを探る
Medidata Platformを知る