リスクベースのSDV
TSDVは、SDVを体系的でリスクに合わせた戦略へと転換します。試験レベルのリスク評価に合わせて、何を、どのレベルで、どこで照合する必要があるかを定義します。
Rave EDCに組み込まれており、重要な安全性および有効性データを完全にカバーしながら、試験ごと、施設ごとに特化したSDV戦略を可能にします。
重要データへの集中
査察への
準備
試験・施設に特化したSDV
フィールドレベルの照合
SDV削減戦略の実践
モニタリングコストの削減
SDVに起因する
モニタリングコストを抑制
100% SDVから脱却し、リスク戦略で求められる箇所にのみ検証を適用します。不要な検証作業や施設訪問を減らすことで、オーバーサイト機能を損なうことなくモニタリングコストを削減できます。
ファクトシートをダウンロード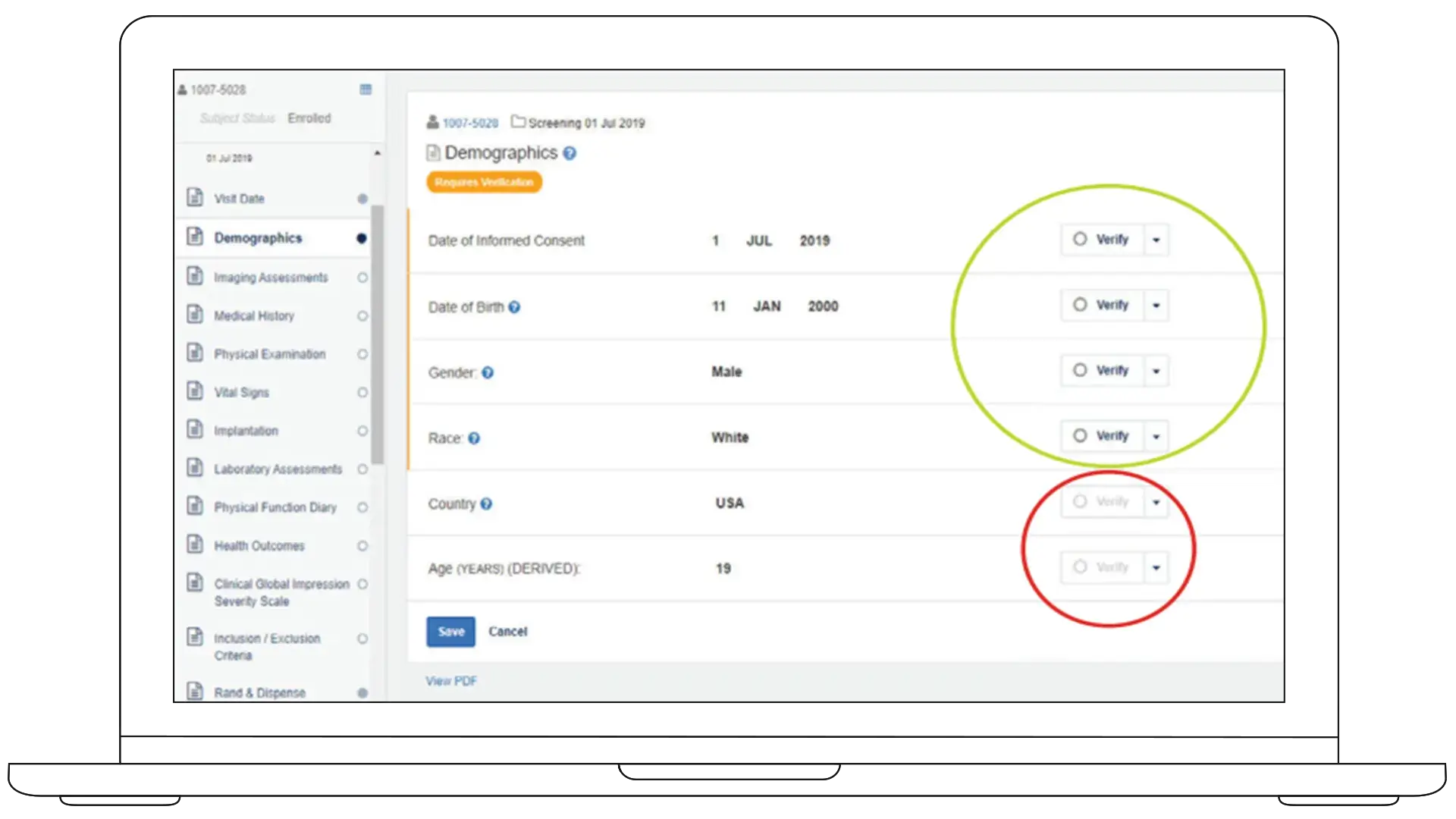
注目のリソース
SDVを50%から目標の15~20%へ
Nordic Bioscienceは、手作業によるSDVの追跡をMedidata TSDVに置き換え、真のリスクベースモニタリングを試験的に導入しました。その結果、業務が効率化され、大幅なコスト削減の可能性とともに、SDVを15~20%にする道筋が立ちました。
導入事例を読む
よくあるご質問
Experiencesを探る
Medidata Platform の詳細


