Medidata CTMS
治験のオーバーサイト業務がスプレッドシートやフォローアップに依存していると、チームは貴重な時間と可視性を失います。
Medidata Clinical Trial Management System (CTMS) は、臨床業務とオペレーション業務を一つの連携したビューに集約し、試験の計画、追跡、オーバーサイトに利用する既存のシステムと連携して機能します。
臨床業務と オペレーション業務を一つに
断片化されたトラッカーではなく、クリックの手間を省き最も重要な情報が明確にされた単一のシステムへ移行しましょう。Medidata CTMSは自動通知でチームに最新情報を提供するように設計され、情報を一度入力すればワークフロー全体でシームレスに再利用できます。
訪問モニタリング
課題管理
オーバーサイト
とレポーティング
文書の提出
と追跡
ICFレビュー
試験管理
Medidata CTMSが選ばれる理由
スケーラブル
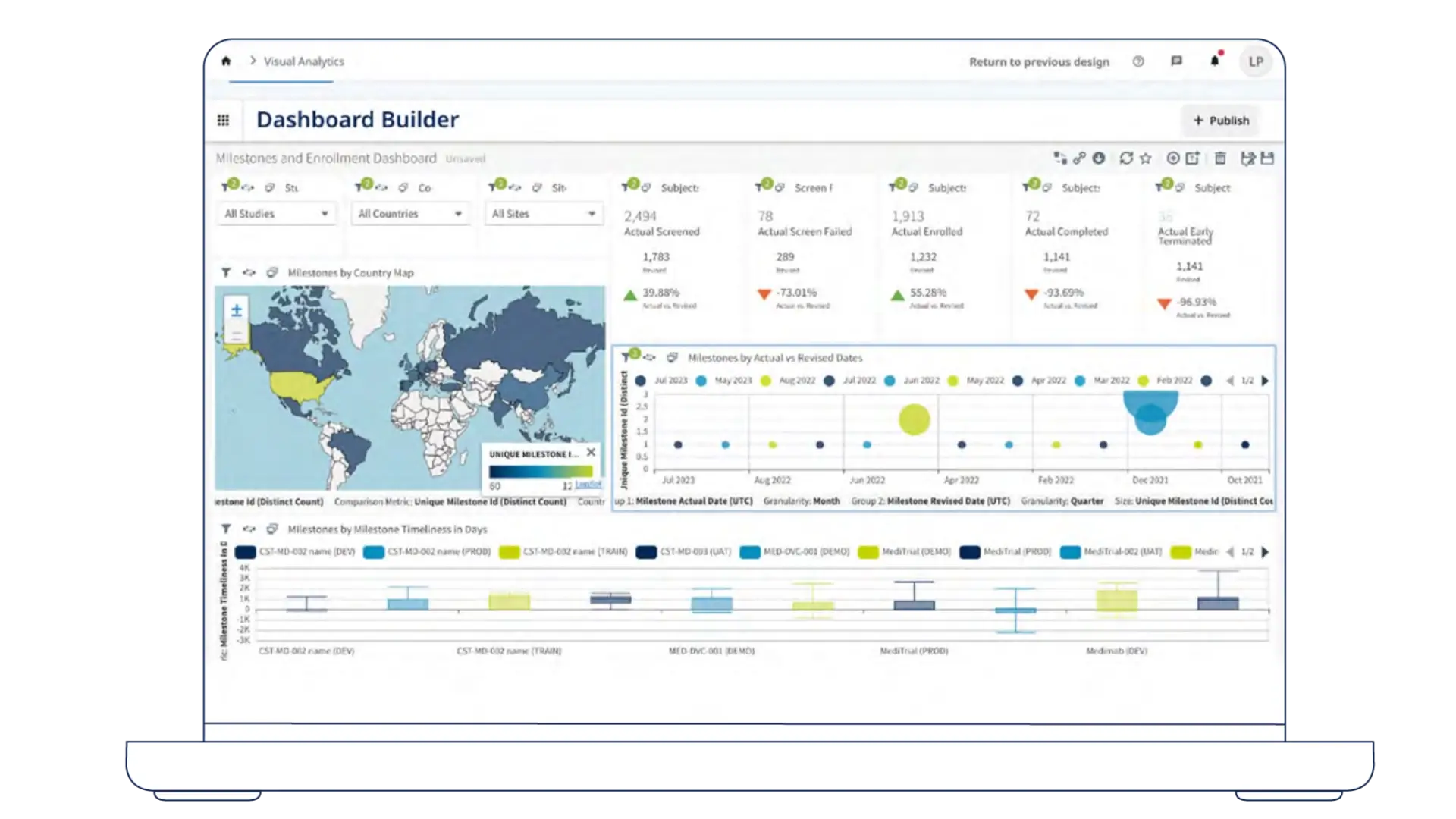
Medidata CTMSによる実証済みの成果
自動化されたワークフローによって少数精鋭チームの効率をさらに向上
ケーススタディをダウンロードケーススタディ
急成長中の製薬企業Enterin社がMedidata CTMSを導入し、リソースに制約のあるチームがより効率的に業務を行えるようになった事例をご覧ください。
「手作業のワークフローを自動化し、すべてのデータを集約することで、Medidata CTMSは当社の臨床試験管理ライフサイクル全体を効率化しました。」

業界での評価
Everest GroupのPEAK Matrix®評価において、13のCTMS製品の中からMedidata CTMSが業界をリードするソリューションとして選ばれました。
Medidata CTMSは、Everest Groupの2024年PEAK Matrix®評価、ライフサイエンス臨床試験管理システム(CTMS)製品部門において、業界のリーダーとして評価されました。


よくあるご質問
Experienceを見る
Medidata Platformの詳細



