Medidata CTMS
임상시험 관리가 스프레드시트나 개별적인 후속 조치에 의존하게 되면, 팀은 귀중한 시간을 허비하고 가시성을 잃게 됩니다.
Medidata Clinical Trial Management System(CTMS)은 임상 및 운영 활동을 하나의 연결된 뷰로 통합하며, 팀이 임상시험을 계획, 추적 및 감독하는 데 사용하는 기존 시스템들과 유기적으로 연동됩니다.
임상과 운영 업무의 통합
분산된 개별 트래커 대신, 클릭 횟수를 줄이고 핵심 정보를 한 눈에 파악하며, 자동 알림으로 팀과 실시간으로 소통할 수 있는 통합 시스템을 만나보세요. 정보를 한 번만 입력하면 모든 워크플로우에서 끊김없이 활용할 수 있습니다.
방문 모니터링
이슈 관리
감독 및 보고
문서 제출 및 추적
ICF 검토
연구 관리
Medidata CTMS를 선택해야 하는 이유
확장성
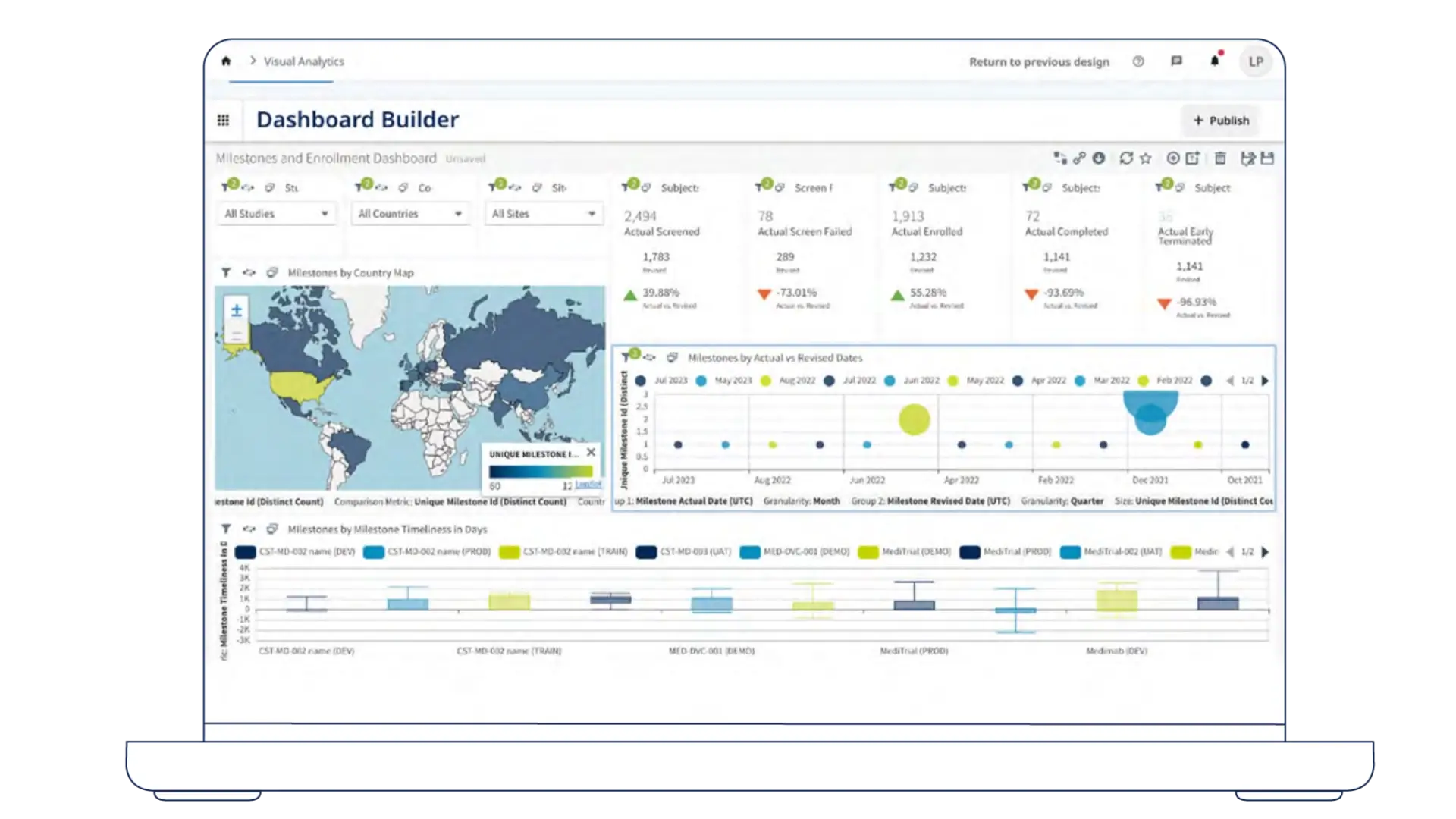
Medidata CTMS의 입증된 결과
워크플로우 자동화로 소규모 팀의 효율성 향상
Case Study 보기Case Study
빠르게 성장 중인 제약사 Enterin이 Medidata CTMS를 도입하여 인력이 제한된 상황에서 어떻게 팀의 업무 효율을 높였는지 확인해 보세요.
"수동 워크플로우를 자동화하고 모든 데이터를 하나로 통합함으로써, Medidata CTMS는 임상시험 관리 라이프사이클 전체를 간소화해주었습니다."

INDUSTRY RECOGNITION
Everest Group이 13개의 CTMS 제품을 대상으로 실시한 PEAK Matrix® 평가에서 Medidata CTMS가 업계 선도적인 솔루션으로 선정.
Medidata CTMS는 Everest Group의 '2024 PEAK Matrix® 생명과학 임상시험 관리 시스템(CTMS) 제품' 부문에서 업계 리더(Industry Leader)로 인정받았습니다.


FAQ
Explore Experiences
Medidata Platform 살펴보기



