Medidata TSDV
시험기관 모니터링 예산의 50% 이상이 근거 데이터 확인(SDV)에 소요됩니다. 하지만 모든 데이터 필드를 일일이 확인하는 방식이 임상 결과에 영향을 미치는 경우는 극히 드뭅니다.
Medidata TSDV (Targeted Source Data Verification)는 Rave EDC 내의 핵심 안전성 및 유효성 데이터에 검토 역량을 집중합니다. 이를 통해 규제 준수에 대한 확신을 유지하면서도 불필요한 업무 노력을 줄여줍니다.
리스크 중심의 SDV 빌드
TSDV는 기존의 SDV 방식을 구조화된 리스크 맞춤형 전략으로 전환합니다. 임상시험 수준의 리스크 평가 결과에 따라, 어떤 데이터를 어느 수준까지, 그리고 어디에서 확인할지 직접 정의할 수 있습니다.
Rave EDC 내부에서 작동하도록 설계되어, 핵심 안전성 및 유효성 데이터를 완벽하게 커버하는 동시에 연구 및 시험 기관별 특성에 맞춘 SDV 전략을 수립할 수 있습니다.
핵심 데이터 포커스
실사 대응 가능 상태 유지
연구 및 기관별 맞춤 SDV
필드 단위 확인
SDV 감축 실전 전략
모니터링 비용 절감
SDV 기반 모니터링 비용 관리
100% SDV 방식에서 벗어나 리스크 전략상 반드시 필요한 부분에만 확인(Verification) 작업을 적용하세요. 불필요한 확인 활동과 시험기관 방문 횟수를 줄임으로써, 관리 감독의 질을 유지하면서도 모니터링 비용을 효과적으로 낮출 수 있습니다.
Fact Sheet 보기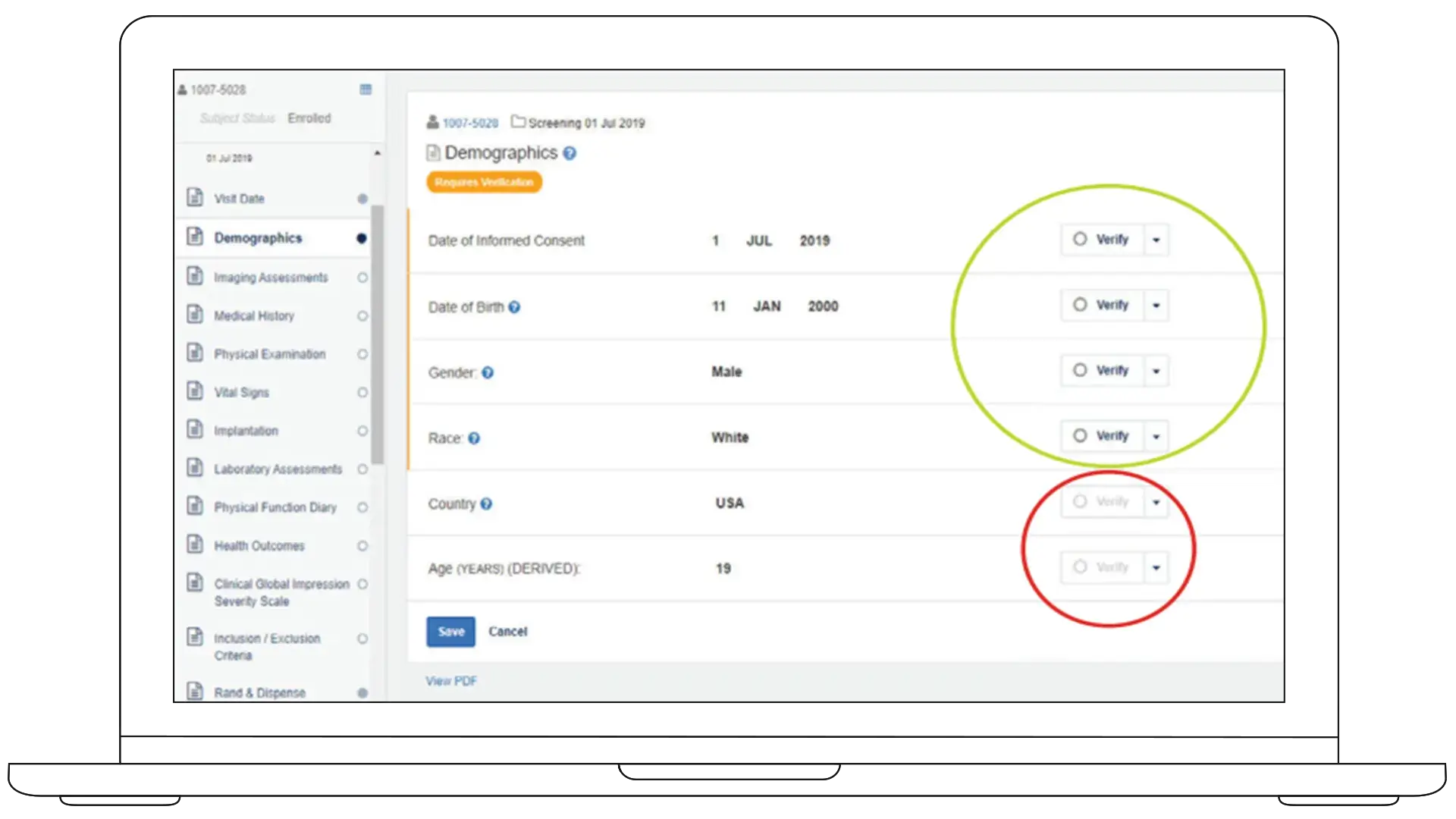
Featured Resource
50%에 달하던 SDV 비율을 전략적인 15~20% 수준으로 감축
Nordic Bioscience는 기존의 수동 SDV 추적 방식을 Medidata TSDV로 대체하고, 진정한 의미의 리스크 기반 모니터링(RBM)을 시범 도입했습니다. 그 결과, 임상 수행 프로세스가 효율화되었으며, SDV 비율을 15~20% 수준으로 낮춤으로써 상당한 비용 절감 가능성을 확인했습니다.

FAQ
Explore Experiences
Medidata Platform 살펴보기


