Site Cloud: End of Study
파일이 흩어져 있거나 수동으로 공유되거나 물리적 매체에 저장된 경우 연구 종료 시 위험이 발생합니다.
Medidata Site Cloud: End of Study(EOS)는 임상시험 종료 시 시험기관 연구 파일을 생성, 배포, 감독할 수 있는 안전한 엔드투엔드(end-to-end) 방식을 제공합니다. 연구 파일은 액세스, 권한, 감사 추적, 실시간 가시성을 중앙에서 관리하는 단일 시스템을 통해 전달되므로 연구 종료에 대한 통제 및 추적성을 확보할 수 있습니다.
연구 종료 시
통제력 유지
수동 인계, 물리적 매체, 분산된 파일은 연구 종료 시 위험을 초래합니다.
Site Cloud: End of Study는 이러한 복잡성을 통제되고 감사 가능한 종료 프로세스로 대체하여 연구 종료 문서를 완전하고 안전하며 실사 대비 상태로 유지합니다.
자동 생성 및 배포
전체 감사 추적
최고 수준의 보안 표준(SOC 2+)
시험기관 만족도 향상
확인을 위한 전자 서명
모든 EOS 파일을 위한 단일 리포지토리
Site Cloud: End of Study를 선택해야 하는 이유
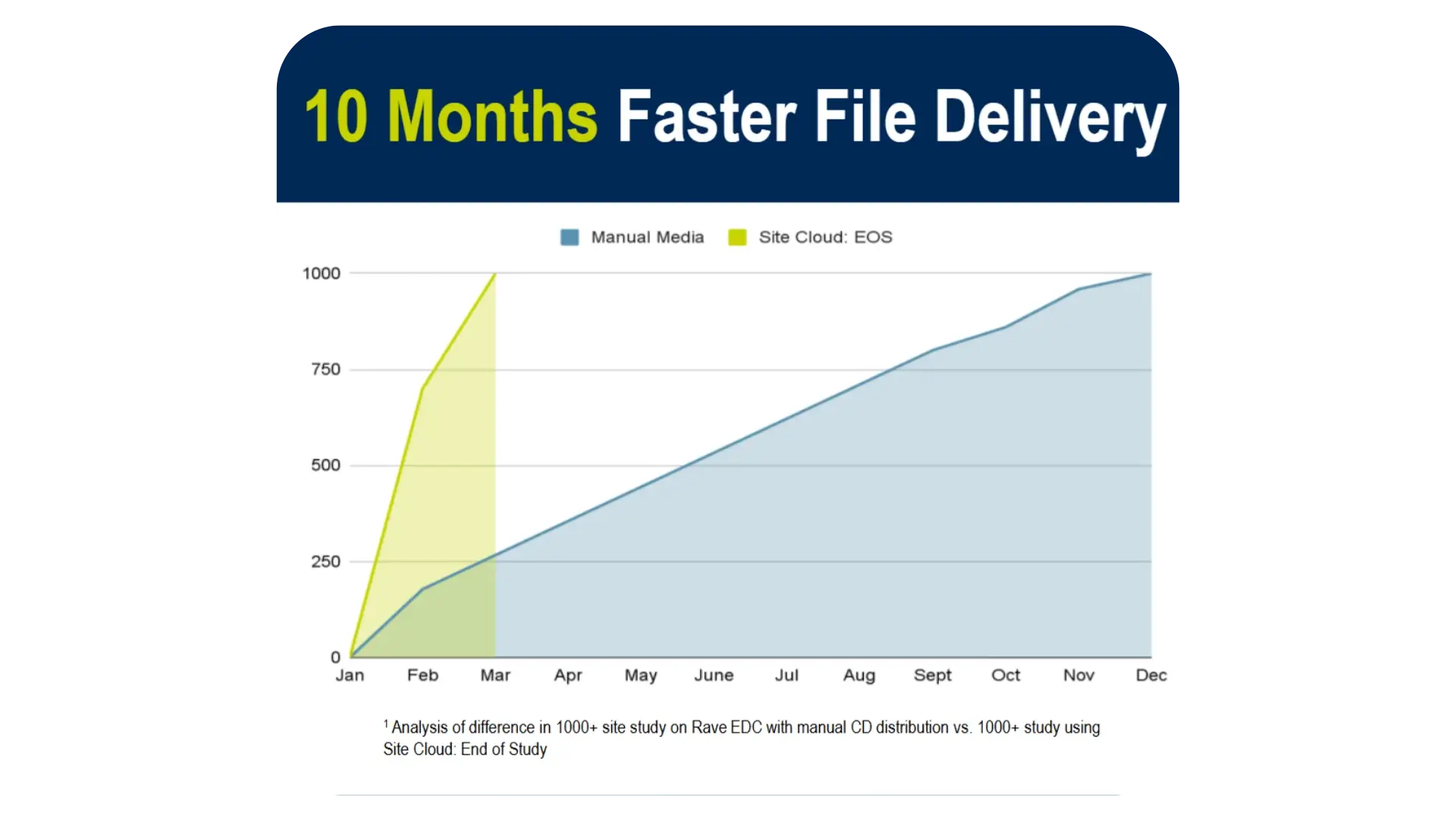
신속한 파일 전달
연구 종료 절차 가속화
미디어는 클라우드에 캡처되어 워크플로우를 간소화합니다.
CD 제작에 드는 시간과 비용을 없애고 데이터에 즉각적이고 안전하게 액세스할 수 있습니다.

FAQ
경험 살펴보기
Medidata 플랫폼 알아보기