围绕风险构建的 SDV
TSDV 将 SDV 转变为一种结构化的、与风险相符的策略。您可以根据研究级别的风险评估,定义需要验证的内容、级别和位置。
它内置于 Rave EDC 中,支持针对特定研究和研究中心的 SDV 策略,同时保持对关键安全性和有效性数据的全面覆盖。
关注关键数据
迎检
就绪
针对特定研究和研究中心的 SDV
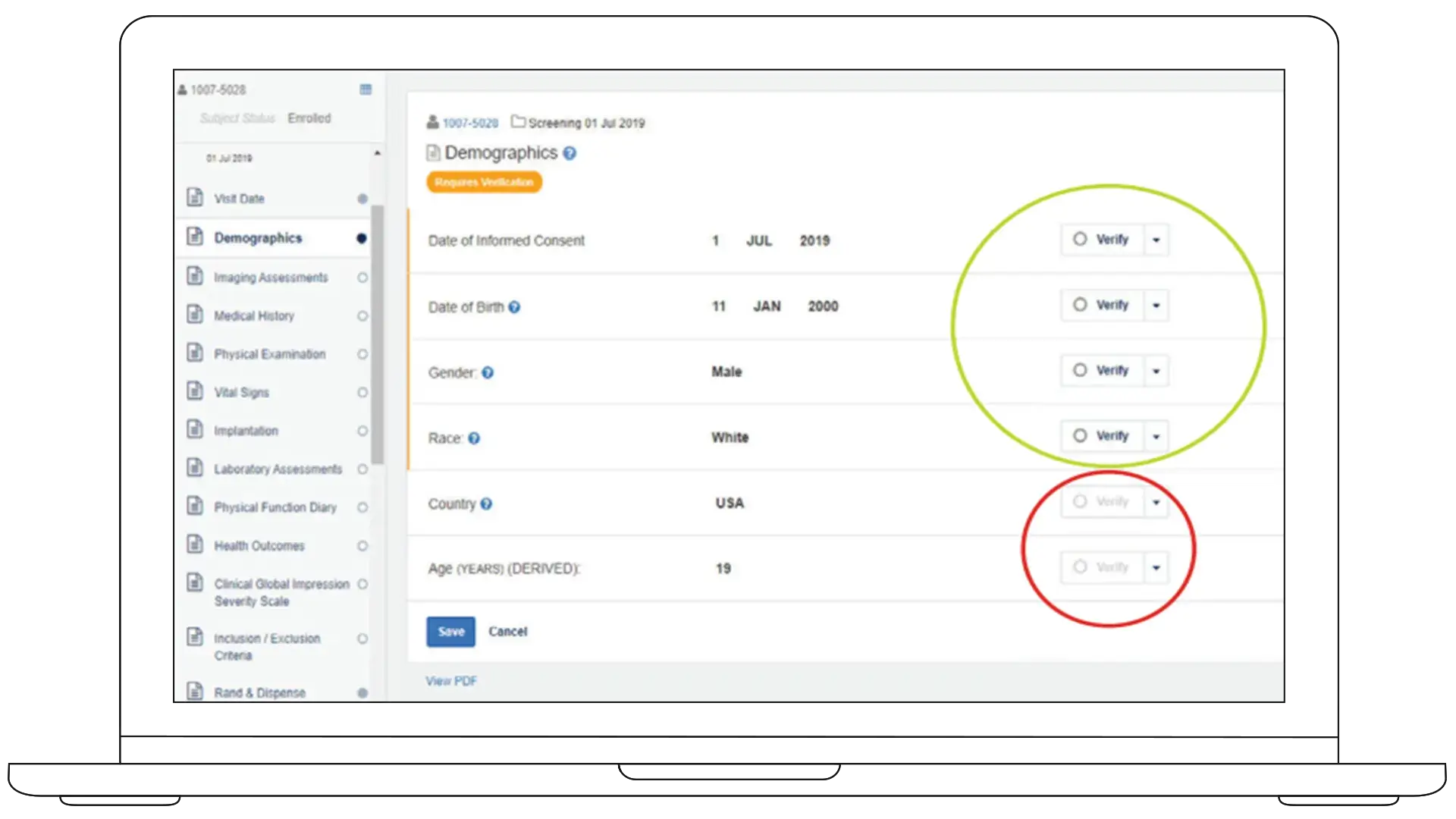
字段级验证
精简 SDV 策略实践
降低监查成本
常见问题
探索体验
探索 Medidata Platform



